2 × Taq PCR MasterMix Ⅱ
Funktioner
■ Høj amplifikationseffektivitet: DNA -fragmenter i forskellige størrelser (lavere end 5 kb) og kilder kan forstærkes effektivt.
■ Høj følsomhed: Så lavt som 10 pg målfragmenter kan forstærkes fra genomiske skabeloner.
■ Høj belastningsmodstand: For skabeloner med et højt urenhedsindhold, f.eks. Råekstraheret skabelon/bakteriekultur, kan målfragmentet let forstærkes. Polymeraseaktiviteten påvirkes ikke af gentagen frysning og optøning.
■ Praktisk til anvendelse: Reaktionssystemet blev klargjort let og hurtigt. Det amplificerede fragment indeholder 3'-ende dA-overhænget, hvilket er praktisk til TA-kloning.
Specifikation
Type: Taq DNA -polymerase
Prøve: Oprenset/ruekstraheret skabelon/bakteriekultur
Skabelon: > 10 sider
Fragmentstørrelse: <5 kb
Ansøgninger: PCR-amplifikation af DNA-fragmenter, DNA-mærkning, primer-forlængelse, sekvensbestemmelse, stor genopdagelse, semi-kvantitativ PCR-eksperimenter, påvisning af spor-DNA osv.
Alle produkterne kan tilpasses til ODM/OEM. For detaljer,klik venligst på Tilpasset service (ODM/OEM)
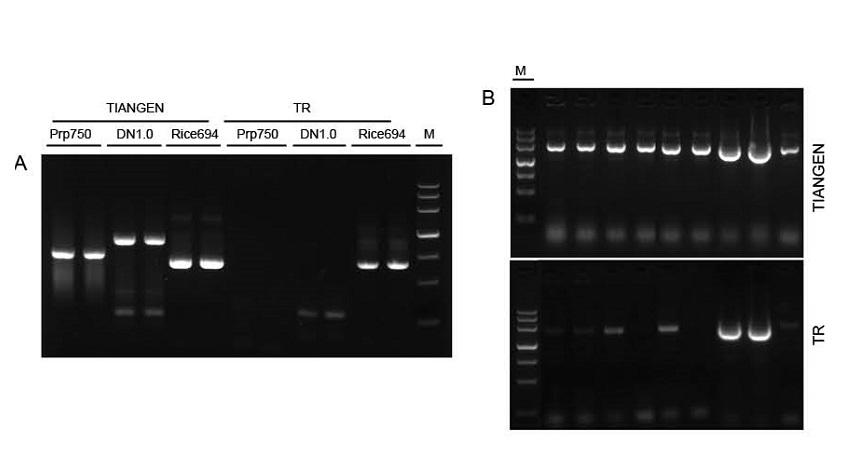 |
Figur 1. Skabeloner fra forskellige kilder blev forstærket af henholdsvis TIANGEN Taq MasterMix II og den fælles Taq Mix fra leverandør TR for at detektere reagensernes modstandsdygtighed over for stress. Resultaterne viser, at TIANGEN -produkter kan forstærke målfragmenterne fra rå genomiske skabeloner og bakteriekultur, og stressresistensen er bedre end hos Supplier TR. A: Rå genomisk skabelon ekstraheret af TIANGEN TIANcombi DNA Lyse & Det PCR Kit. Prp/DN: Råekstraktion og påvisning af humane blodprøver. Ris: Råekstraktion og påvisning af risprøver. B: Koloni PCR. PCR -fragmentet er 700 bp. M: TIANGEN Marker III |
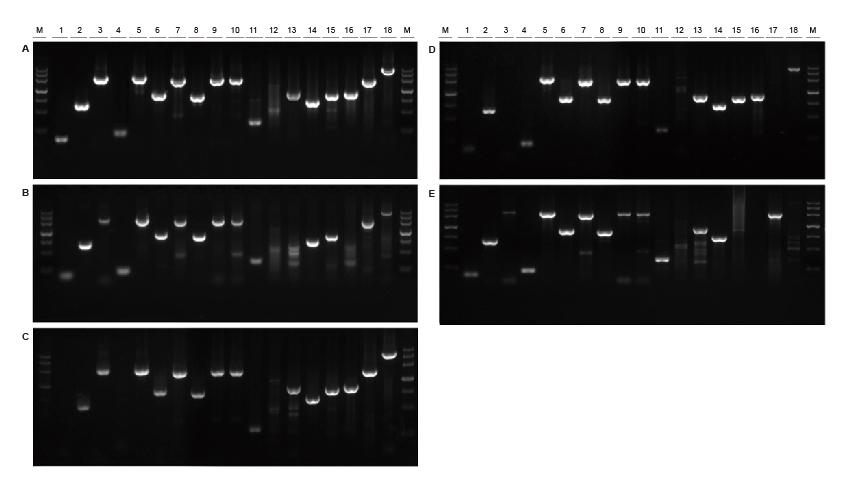 |
God universalitet til skabeloner fra forskellige kilder og med forskellige længder Figur 2. Fragmenter af forskellige kilder og længder blev amplificeret under anvendelse af TIANGEN Taq MasterMix II (A) og almindelig Taq Blanding af henholdsvis Supplier TK (B), Supplier TR (C), Supplier V (D) og Supplier G (E). Resultaterne viser, at den omfattende ydelse af TIANGEN -produkter er den bedste med hensyn til amplifikationsevne, specificitet og universalitet.M: TIANGEN Marker III1: Soybean genomic DNA template (120 bp); 2-3: Ris genomisk DNA-skabelon (694 bp, 2258 bp); 4: Genomisk DNA -skabelon af bomuld (200 bp); 5: Escherichia coli genomisk DNA -skabelon (2298 bp); 6-7: Musgenoms DNA-skabelon (1 kb, 2 kb); 8-10: Rotte genomisk DNA-skabelon (1 kb, 2 kb, 2080 bp); 11-18: DNA-skabelon for humant genom (300 bp, 448 bp (GC%: 74,8%), 1100 bp, 750 bp, 1000 bp, 1090 bp (GC%: 70,4%), 2 kb, 4 kb) |
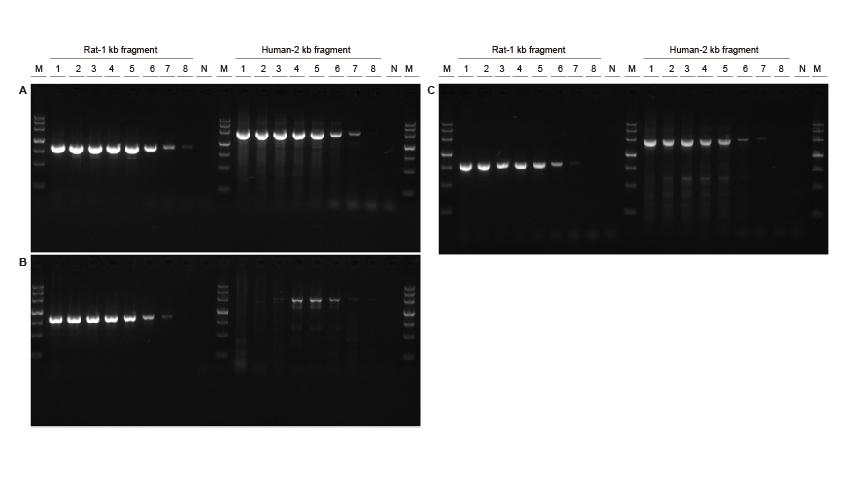 |
Høj følsomhed Figur 3. Forskellige koncentrationer af rotte- og humane DNA -fragmenter blev amplificeret under anvendelse af TIANGEN Taq MasterMix II (A), almindelig Taq Blanding af henholdsvis leverandør V (B) og leverandør TK (C) for at detektere forstærkningsfølsomheden. Resultaterne viser, at TIANGEN-produktet kunne forstærke målfragmentet fra genomskabelonen så lavt som 0,01 ng, og dets følsomhed er bedre end produkterne fra leverandør V og TK.M: TIANGEN Marker III, N: NTC Skabelonindgang 1-8 : 200 ng, 100 ng, 50 ng, 20 ng, 10 ng, 1 ng, 0,1 ng, 0,01 ng. |
A-1 skabelon
■ Skabelonen indeholder protein -urenheder eller Taq -hæmmere osv. —— Rens DNA -skabelon, fjern protein -urenheder eller ekstraher skabelon -DNA med oprensningssæt.
■ Denatureringen af skabelonen er ikke fuldført —— Forøget denatureringstemperatur passende og forlæng denatureringstiden.
■ Nedbrydning af skabeloner —— Forbered skabelonen igen.
A-2 Primer
■ Dårlig kvalitet af primere —— Re-syntetisere primeren.
■ Nedbrydning af primer —— Alikvoter primerne med høj koncentration i lille volumen til konservering. Undgå flere frysninger og optøninger eller langtids 4 ° C kryokonserveret.
■ Ukorrekt udformning af primere (f.eks. Primerlængde ikke tilstrækkelig, dimer dannet mellem primere osv.) -Rediger primere (undgå dannelse af primer -dimer og sekundær struktur)
A-3 mg2+koncentration
■ Mg2+ koncentrationen er for lav —— Korrekt stigning Mg2+ koncentration: Optimer Mg2+ koncentration ved en række reaktioner fra 1 mM til 3 mM med et interval på 0,5 mM for at bestemme den optimale Mg2+ koncentration for hver skabelon og primer.
A-4 Udglødningstemperatur
■ Den høje udglødningstemperatur påvirker bindingen af primer og skabelon. —— Reducer udglødningstemperaturen, og optimer tilstanden med en gradient på 2 ° C.
A-5 Forlængelsestid
■ Kort forlængelsestid —— Forlæng forlængelsestiden.
Fænomener: Negative prøver viser også målsekvensbåndene.
A-1 Forurening af PCR
■ Krydsforurening af målsekvens eller amplifikationsprodukter —— Forsøg ikke at pipette prøven, der indeholder målsekvensen, i den negative prøve eller spilde dem ud af centrifugerøret. Reagenserne eller udstyret skal autoklaveres for at fjerne eksisterende nukleinsyrer, og forekomsten af kontaminering bør bestemmes gennem negative kontrolforsøg.
■ Kontaminering af reagenser —— Alikvoter reagenserne, og opbevar dem ved lav temperatur.
A-2 Primer
■ Mg2+ koncentrationen er for lav —— Korrekt stigning Mg2+ koncentration: Optimer Mg2+ koncentration ved en række reaktioner fra 1 mM til 3 mM med et interval på 0,5 mM for at bestemme den optimale Mg2+ koncentration for hver skabelon og primer.
■ Forkert primerdesign, og målsekvensen har homologi med ikke-målsekvensen. —— Re-design primere.
Fænomener: PCR-amplifikationsbåndene er uforenelige med den forventede størrelse, enten store eller små, eller nogle gange forekommer både specifikke amplifikationsbånd og uspecifikke amplifikationsbånd.
A-1 Primer
■ Dårlig primerspecificitet
—— Re-design primer.
■ Primer -koncentrationen er for høj —— Forøg korrekt denatureringstemperaturen og forlæng denatureringstiden.
A-2 mg2+ koncentration
■ Mg2+ koncentrationen er for høj —— Reducer Mg2+ -koncentrationen korrekt: Optimer Mg2+ koncentration ved en række reaktioner fra 1 mM til 3 mM med et interval på 0,5 mM for at bestemme den optimale Mg2+ koncentration for hver skabelon og primer.
A-3 termostabil polymerase
■ Overdreven enzymmængde —— Reducer enzymmængden passende med intervaller på 0,5 U.
A-4 Udglødningstemperatur
■ Glødningstemperaturen er for lav —— Hæv glødetemperaturen passende, eller anvend to-trins glødemetoden
A-5 PCR-cyklusser
■ For mange PCR -cykler —— Reducer antallet af PCR -cyklusser.
A-1 Primer——Dårlig specificitet —— Gendesign primeren, ændr primerens position og længde for at forbedre dens specificitet; eller udføre indlejret PCR.
A-2 Skabelon-DNA
——Skabelonen er ikke ren —— Rens skabelonen, eller udtræk DNA med rensningssæt.
A-3 mg2+ koncentration
——Mg2+ koncentrationen er for høj —— Reducer Mg korrekt2+ koncentration: Optimer Mg2+ koncentration ved en række reaktioner fra 1 mM til 3 mM med et interval på 0,5 mM for at bestemme den optimale Mg2+ koncentration for hver skabelon og primer.
A-4 dNTP
—— Koncentrationen af dNTP’er er for høj —— Reducer koncentrationen af dNTP på passende vis
A-5 Udglødningstemperatur
——For lav udglødningstemperatur —— Forøg passende udglødningstemperatur
A-6 cykler
——For mange cykler ——Optimér cyklustallet

Det første trin er at vælge den passende polymerase. Regelmæssig Taq-polymerase kan ikke korrekturlæses på grund af mangel på 3'-5 'exonukleaseaktivitet, og mismatch vil i høj grad reducere forlængelseseffektiviteten af fragmenter. Derfor kan almindelig Taq -polymerase ikke effektivt amplificere målfragmenter større end 5 kb. Taq -polymerase med særlig modifikation eller anden højfidelitetspolymerase bør vælges for at forbedre forlængelseseffektivitet og opfylde behovene ved langfragmentforstærkning. Derudover kræver amplifikation af lange fragmenter også tilsvarende justering af primerdesign, denatureringstid, forlængelsestid, buffer-pH osv. Normalt kan primere med 18-24 bp føre til bedre udbytte. For at forhindre skabelonskade bør denatureringstiden ved 94 ° C reduceres til 30 sekunder eller mindre pr. Cyklus, og tiden til at stige temperaturen til 94 ° C før forstærkning bør være mindre end 1 min. Desuden kan indstilling af forlængelsestemperaturen til ca. 68 ° C og design af forlængelsestiden i henhold til hastigheden på 1 kb/min sikre effektiv forstærkning af lange fragmenter.
Fejlhastigheden ved PCR -amplifikation kan reduceres ved anvendelse af forskellige DNA -polymeraser med høj kvalitet. Blandt alle de Taq DNA -polymeraser, der er fundet indtil nu, har Pfu -enzym den laveste fejlrate og den højeste troværdighed (se vedhæftede tabel). Ud over enzymudvælgelse kan forskere yderligere reducere PCR -mutationshastighed ved at optimere reaktionsbetingelser, herunder optimering af buffersammensætning, koncentration af termostabil polymerase og optimering af PCR -cyklustal.
Produkter kategorier
HVORFOR VÆLGE OS
Siden etableringen har vores fabrik udviklet produkter i verdensklasse med overholdelse af princippet
af kvalitet først. Vores produkter har opnået et fremragende ry i branchen og er værdifulde blandt nye og gamle kunder.








